理論要完全看透的話,也許需要唸個化學學士,寶石學範疇內只涉及較淺易的知識,簡略明白其中幾個重點機制和例子。理解了大致上的顯色機理就能順道搞懂一些常見寶石人造和優化 / 加工過程,比如說剛玉和綠柱石的加熱處理,檢測出染色祖母綠和翡翠等。
看到這裡已經想打瞌睡的同學們可以直接跳去噗尾看《寶石學講義》的節錄文章
看到這裡已經想打瞌睡的同學們可以直接跳去噗尾看《寶石學講義》的節錄文章
過往兩期都圍繞著晶場理論,以單一原子中的電子軌道分裂,電子在能階之間的跳躍產生電磁波並進入可見光範圍,去理解一些礦石顏色的形成。這次將會在晶體結構中加入分子軌道理論去解構顏色的起因,該理論中的電子不受限於原子之間的化學鍵,而是受整個分子的原子核影響並圍繞分子運動。
先複習一下上兩期講到的晶場理論,晶體構成原子中電子的一些知識:
*光和其他電磁波以光子的形式發射 / 吸收
*光和電子可以相互作用和交換能量
*晶體原子中的電子每個都擁有一定的能量
*如果向晶體增加更多的能量,電子可被激發並轉移到更高的能階
以上都是以單一原子來看待能階,但我們都知道晶體是由許多週期性的微粒子單元而排列而成。
而這些微粒子單元會由不同電荷間的吸引力聯成為固體,相互作用常涉及原子或分子最外層的電子。
先複習一下上兩期講到的晶場理論,晶體構成原子中電子的一些知識:
*光和其他電磁波以光子的形式發射 / 吸收
*光和電子可以相互作用和交換能量
*晶體原子中的電子每個都擁有一定的能量
*如果向晶體增加更多的能量,電子可被激發並轉移到更高的能階
以上都是以單一原子來看待能階,但我們都知道晶體是由許多週期性的微粒子單元而排列而成。
而這些微粒子單元會由不同電荷間的吸引力聯成為固體,相互作用常涉及原子或分子最外層的電子。
化學鍵合
常見寶石中主要為原子晶體和離子晶體類型為主,因此原子間構成化學鍵的作用力我們主要看共價鍵和離子鍵。 這些鍵類型中的兩種或多種可以在大多數礦物中共存,並決定了其物理和化學特性(有興趣的旅人可以自己搜搜看深入瞭解)。
不同的元素試圖結合形成分子時,具有最高電負性的元素是最霸道的,優先於具有較低電負性的元素。「貪婪的」元素從另一個元素中奪取了帶負電荷的電子,因此具有了額外的負電荷而變成陰離子;而放出電子的元素則變成帶正電的陽離子。元素之間發生極化,就像一塊磁鐵把兩個元素吸引在一起。換句話說,它們形成了牢固的鍵,並且會有電子的交換(捐贈和接收)。這被稱為離子鍵。
常見寶石中主要為原子晶體和離子晶體類型為主,因此原子間構成化學鍵的作用力我們主要看共價鍵和離子鍵。 這些鍵類型中的兩種或多種可以在大多數礦物中共存,並決定了其物理和化學特性(有興趣的旅人可以自己搜搜看深入瞭解)。
不同的元素試圖結合形成分子時,具有最高電負性的元素是最霸道的,優先於具有較低電負性的元素。「貪婪的」元素從另一個元素中奪取了帶負電荷的電子,因此具有了額外的負電荷而變成陰離子;而放出電子的元素則變成帶正電的陽離子。元素之間發生極化,就像一塊磁鐵把兩個元素吸引在一起。換句話說,它們形成了牢固的鍵,並且會有電子的交換(捐贈和接收)。這被稱為離子鍵。

藍色剛玉(Blue corundum)

在晶場理論篇提到過,雜質元素鉻替代了剛玉晶體 Al₂O₃ 結構中的一部分的鋁離子時,便會引起紅寶石的顏色。*見附錄(一)
1902 年,在宣布成功用焰熔法複製紅寶石後不久,伐諾伊教授就嘗試複製藍寶石。 但鈷,跟一系列的雜質元素,也沒有使 Al₂O₃ 呈現出藍色。 當在分析天然藍寶石的成分時,他觀察到所有藍寶石都含有微量的鐵和鈦氧化物,缺一不可。 只含鈦(Ti)離子的話,晶體會顯示為無色;如含有相同份量的鐵(Fe)離子,晶體會呈現淡黃色。確實顯色機制也讓科學家尋思了大概六十年,到1970年才被正式結論為:兩種雜質同時出現並進行電荷轉移,吸收大量光子能量,從而產生非常強烈的藍色。
在晶場理論篇提到過,雜質元素鉻替代了剛玉晶體 Al₂O₃ 結構中的一部分的鋁離子時,便會引起紅寶石的顏色。*見附錄(一)
1902 年,在宣布成功用焰熔法複製紅寶石後不久,伐諾伊教授就嘗試複製藍寶石。 但鈷,跟一系列的雜質元素,也沒有使 Al₂O₃ 呈現出藍色。 當在分析天然藍寶石的成分時,他觀察到所有藍寶石都含有微量的鐵和鈦氧化物,缺一不可。 只含鈦(Ti)離子的話,晶體會顯示為無色;如含有相同份量的鐵(Fe)離子,晶體會呈現淡黃色。確實顯色機制也讓科學家尋思了大概六十年,到1970年才被正式結論為:兩種雜質同時出現並進行電荷轉移,吸收大量光子能量,從而產生非常強烈的藍色。
鐵和鈦在 Al₂O₃ 結構中都取代了(Al)鋁,位於一個稍微扭曲的六氧八面體內部。鐵和鈦都可以以兩種價態存在,因此在結構中能以兩種組合形式存在: (a) Fe²ᐩ 和 Ti⁴ᐩ; (b ) Fe³ᐩ 和 Ti³ᐩ。如果 Fe²ᐩ 和 Ti⁴ᐩ 都存在,並位於相鄰的 Al 位點上,它們就有可能建立相互作用。
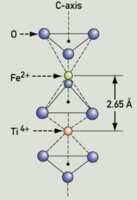
(圖A)
從以上的圖能看到這種晶體配置的兩個八面體沿著 C軸 方向上共享表面。這種排列中,相鄰的 Fe 和 Ti 離子相距很近,離子的軌道有足夠的重疊,以至於電子可以從一個離子傳遞到另一個離子。通過失去一個電子,Fe²ᐩ 會氧化為 Fe³ᐩ,而Ti⁴ᐩ 獲得電子會還原為 Ti³ᐩ,如下所示:
Fe²ᐩ + Ti⁴ᐩ → Fe³ᐩ + Ti³ᐩ
(圖A)
從以上的圖能看到這種晶體配置的兩個八面體沿著 C軸 方向上共享表面。這種排列中,相鄰的 Fe 和 Ti 離子相距很近,離子的軌道有足夠的重疊,以至於電子可以從一個離子傳遞到另一個離子。通過失去一個電子,Fe²ᐩ 會氧化為 Fe³ᐩ,而Ti⁴ᐩ 獲得電子會還原為 Ti³ᐩ,如下所示:
Fe²ᐩ + Ti⁴ᐩ → Fe³ᐩ + Ti³ᐩ
(圖B)
*氧化態的升高稱為氧化,降低則稱為還原。
*還原是獲得電子的過程,而氧化是失去電子的過程。
這種新組合 Fe³ᐩ + Ti³ᐩ 的能量比 Fe²ᐩ + Ti⁴ᐩ 高出 2.11eV; 由此產生的能級方案如(圖C)所示。如果這種能量的光落在藍寶石上,它會被吸收,同時產生方程式 Fe²ᐩ + Ti⁴ᐩ → Fe³ᐩ + Ti³ᐩ 的電荷轉移,這個過程也被稱為氧化還原。 由此產生的寬吸收區可以在 (圖D) 的上部曲線中看到。 (圖A)的晶體配置,和(圖B)的相互作用方程式適用於尋常光「o光」(垂直於 C軸 偏振的光)。 電子最終會吸收黃光到紅光波段的部份,使得藍寶石呈現深藍色。
由於涉及兩種不同的金屬,所以又叫異核間隔電荷轉移。
綠柱石的金黃品種,主要以結構中的鐵雜質離子 Fe³ᐩ 著色。 Fe³ᐩ 離子的躍遷僅吸收光譜的藍色和紫色部分;它們非常弱,並且對顏色的貢獻很小。而我們看到的深黃色卻是由以紫外線為中心的極強吸收引起的,該吸收延伸到可見光譜的藍色端並吸收紫色和藍色。這種紫外線吸收不僅是因為 Fe³ᐩ,而是由 Fe³ᐩ 與綠柱石結構中的氧鄰居之間的相互作用產生的。顏色是由通過電子從氧離子轉移到鐵離子然後吸收的光而形成,這種顏色也可以通過照射海藍寶人為誘發。
前面介紹藍寶石的章節解釋過,涉及兩種不同的金屬叫異核電荷轉移。當離子屬於同一元素時,會發生同核電荷轉移。一個常見的例子是在 Fe 中發生的轉變。同核間隔電荷轉移顏色源自——單個過渡元素中不同價態的兩個原子之間的相互作用。如果鐵的兩種常見價態: Fe²ᐩ 和 Fe³ᐩ 離子在絕緣晶體中佔據相鄰的相同位置,將一個電子從 Fe²ᐩ 移動到 Fe³ᐩ 以反轉它們的電荷狀態;這移動本身不會涉及能量變化,因為最終狀態和初始狀態一樣,因此該過程不會導致光的吸收。但是,如果兩個鐵離子位於不同類型的位置,兩種排列之間則會存在能量差異。
概括
與晶場理論一樣,分子群的點對稱性和幾何畸變以及鍵合強度是重要的參數。電荷轉移產生異常激烈的吸收,因為選擇定則完全允許轉換,躍遷具有高躍遷概率,因此產生強烈的顏色,並且當兩者都存在時往往會主導晶場躍遷顏色,儘管它們也可能發生在光譜的紫外部分(人類不可見)的地方。
間隔電荷轉移涉及在兩個可變價過渡金屬離子間轉移的電子,成色通常是棕色、深藍色或黑色。而且還有一個有趣特徵是其極端的方向性,這通常會導致強烈的多色性。 例如,由於離子偶的方向,海藍寶中的 Fe²ᐩ-Fe³ᐩ 在「e光」軸方向最顯色。 這就是為什麼切磨師要將工作台切面與光軸垂直,才能在海藍寶中獲得盡可能最深的顏色。 在堇青石中的多色性(紫 / 藍 / 黃),也是順著「o光」軸方向最能觀察到 Fe²ᐩ-Fe³ᐩ 的電荷轉移。
與晶場理論一樣,分子群的點對稱性和幾何畸變以及鍵合強度是重要的參數。電荷轉移產生異常激烈的吸收,因為選擇定則完全允許轉換,躍遷具有高躍遷概率,因此產生強烈的顏色,並且當兩者都存在時往往會主導晶場躍遷顏色,儘管它們也可能發生在光譜的紫外部分(人類不可見)的地方。
間隔電荷轉移涉及在兩個可變價過渡金屬離子間轉移的電子,成色通常是棕色、深藍色或黑色。而且還有一個有趣特徵是其極端的方向性,這通常會導致強烈的多色性。 例如,由於離子偶的方向,海藍寶中的 Fe²ᐩ-Fe³ᐩ 在「e光」軸方向最顯色。 這就是為什麼切磨師要將工作台切面與光軸垂直,才能在海藍寶中獲得盡可能最深的顏色。 在堇青石中的多色性(紫 / 藍 / 黃),也是順著「o光」軸方向最能觀察到 Fe²ᐩ-Fe³ᐩ 的電荷轉移。
*補充一下那個強烈對比:
紅寶石晶體內需要含有1%的鉻離子去產生深邃的紅色;但藍寶石的鐵和鈦含量只需達0.01%。加上相對紅寶石的禁阻,藍寶石的電子躍遷是允許的,因此成色比一般金屬離子致色能來得100至1000倍強烈。
紅寶石晶體內需要含有1%的鉻離子去產生深邃的紅色;但藍寶石的鐵和鈦含量只需達0.01%。加上相對紅寶石的禁阻,藍寶石的電子躍遷是允許的,因此成色比一般金屬離子致色能來得100至1000倍強烈。
 LikeCoin - Reinventing the Like
LikeCoin - Reinventing the Like覺得科普有用的話,可點擊以上連結按讚一到五次,化讚為賞,我就會得到 Like coin 的回饋
回饋由 likecoin 基金會出資,只需註冊並登入帳號,不用花錢只需點讚,便能贊助我的心血,謝謝支持~
===================================
掙扎了很久該怎樣拆小分題,改了好幾遍順序還是覺得思路有點跳躍,啊啊大自然熔爐把一堆元素煉成的結果就是很多東西都模糊不清呢。我下一篇要不要先跳過帶隙理論啊(痛哭),先寫比較好玩的物理特性好了。
關於多色性,請到我的置頂噗爬文謝謝